生物科学自发召回所有ION*Sinus支持、ION*BiomeSinus和恢复Sinus喷射产品消费者级FDA测试发现产品内含微菌分片、Fictibacillus分片、Bacillus分片等微生物沾染marikii和peenibacillusspe
风险说明:在风险最大的人群中,最近接受鼻线或鼻线外科手术的病人或个人中,使用受影响产品有合理概率可能导致严重或威胁生命的不良事件,如白血病或真菌病、入侵性细菌或真菌犀牛炎或传播真菌感染生物科学迄今尚未收到任何与该产品有关的不良事件报告
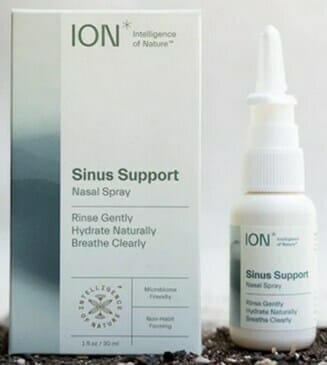
产品用作鼻喷槽并打包成一两个鼻喷喷器单盒(见下文产品图片)。
产品名 |
销售周期 |
ION*sinus支持 |
2021年9月20日至2023年9月20日 |
INO*BiomeSinus |
2019年9月至2021年9月 |
恢复Sinus喷射 |
2017年6月至2019年9月 |
受影响批量分布到批发商店并直接在线售给消费者
生物科学通过电子通讯通知经销商和客户并安排处置所有回调产品,消费者和有回调产品的其他方应停止使用产品并丢弃产品或照相瓶底部批号后再丢弃并规定生物科学安排退款(下文提供联系信息)。
问题方可联系ION*Sinus回召团队,时间为1-844-715-0113周一-周五九点到五点东部时间或sinusrecall@intelligenceofnature.com.消费者如果遇到可能与获取或使用该产品有关的问题,应联系他们的医生或保健提供者。
使用该产品时遇到的不利反应或质量问题可在线或普通邮件或传真向FD MedWatch反事件报告程序报告
- 完成并提交报表在线:www.fda.gov/medwatch/report.htm
- 正则邮件或传真:下载表单www.fda.gov/MedWatch/getforms.htm或调用1-800-332-1088请求报告表,然后填回预地址表或传真提交1-800-FDA-0178
召回程序使用美国知识食品药管局